Карбоновые кислоты — это органические соединения, которые несут одну или несколько карбоксильных групп (–COOH). Соли называются карбоксилатами, а сложные эфиры — эфирами карбоновых кислот.
Характерной особенностью молекулы карбоновой кислоты является группа -СООН, карбоксигруппа (карбоксильная группа). Насыщенные карбоновые кислоты без двойных связей в углеродном скелете являются насыщенными, их называют алкановыми кислотами.
Многие соединения обладают бессистемными именами (имеют тривиальные названия), которые заканчиваются словом «кислота», а само название может указывать из какого именно вещества была получена кислота (муравьиная кислота, масляная кислота, лимонная кислота и т.д.). Когда они связаны с другими элементами, такими как водород, кислород или азот, то могут образовывать бесконечное количество различных соединений.
Карбоновые кислоты содержат большую группу органических кислот, которые широко распространены в природе. В чистом виде некоторые из карбоновых кислот обладают сильным едким и токсическим действием, но в жизни мы поглощаем небольшие количества через пищу: квашеная капуста сбраживается молочной кислотой, виноград содержит натуральную винную кислоту, все цитрусовые содержат лимонную кислоту, а яблоки и груши — яблочную кислоту.
Эти кислоты классифицируются в соответствии с количеством карбоксильных групп:
Различают алифатические, ароматические и гетероциклические карбоновые кислоты, в соответствии с химической структурой радикала, к которому присоединена группа -COOH:
- Алкановые кислоты, также называют насыщенными карбоновыми кислотами;
- Алкеновые кислоты, карбоновые кислоты с по меньшей мере одной двойной связью;
- Алкиновые кислоты с по меньшей мере одной тройной связью.
Карбоновые кислоты также могут быть дифференцированы в зависимости от количества карбоксильных групп. Монокарбоновые кислоты имеют одну карбоксильную группу, дикарбоновые — две, а трикарбоновые — три.
- Монокарбоксилат, молекула содержит одну карбоксильную группу, такую как муравьиная, уксусная, пальмитиновая, стеариновая, валериановая кислота.
- Дикарбоновый, каждый атом включает две карбоновые группы, включая щавелевую кислоту, малоновую, глутаровую, адипиновую, пимелиновую, себациновую.
- Трикарбоновая или поликарбоновая, одна частица имеет три карбоксильные группы, прототипом которых является лимонная кислота.
Жирные кислоты представляют собой неразветвленные алифатические монокарбоновые кислоты с по меньшей мере 4 атомами углерода.
- алифатические, насыщенные монокарбоновые кислоты: Уксусная кислота, Масляная кислота;
- алифатические ненасыщенные монокарбоновые кислоты: Акриловая кислота, Олеиновая кислота;
- алифатические, насыщенные дикарбоновые кислоты: Щавелевая кислота, Янтарная кислота;
- алифатические ненасыщенные: Лимонная кислота;
- дикарбоновые кислоты: Фумаровая кислота, Малеиновая кислота;
- ароматические карбоновые кислоты: Бензойная кислота, Салициловая кислота;
- гетероциклические карбоновые кислоты: Никотиновая кислота;
- алифатические, ненасыщенные, циклические монокарбоновые кислоты: Абиетиновая кислота (смоляная кислота).
Химические и физические свойства карбоновых кислот
Химические и физические свойства карбоновых кислот четко определяются наличием карбоксильной группы. Именно карбоксильная группа позволяет высвобождать ионы H +, например, уксусной кислоты:
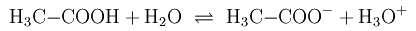
Карбоновые кислоты с короткой цепью представляют собой бесцветные жидкости с сильным запахом. Благодаря карбоксильной группе, они имеют полярный характер, что приводит к относительно высоким температурам кипения за счет водородных связей.
С увеличением длины цепи, липофильный характер увеличивается, а гидрофильный характер уменьшается. Это относится и к солям карбоновых кислот. Молекулы наиболее распространенных жирных кислот имеют 16 или 18 атомов углерода.
Качества характеризующие карбоновые кислоты:
- Как правило, являются твердыми и содержат более восьми атомов углерода, если отсутствует двойная связь, которая предотвращает компактное образование.
- Постепенно, по мере роста углеродной цепи уменьшается их растворимость в воде и наоборот повышается растворимость в спиртах.
- С гидроксильной группой они образуют водородную кислоту и ведут себя как основания и имеют более высокую температуру кипения, чем спирты, кетоны или альдегиды из-за высокого содержания водорода.
- Реагируют с натриевыми солями щелочного происхождения, которые используются при производстве мыла.
- При реакции со спиртами дают сложные эфиры — соединения, которые могут образовывать большое количество фруктовых ароматов.
- С органической кислотой они теряют воду, что вызывает эффект шипучести в напитках в прохладительных напитках.
- Становятся кислыми хлоридами при контакте с тионилом и оксалилхлоридом, образуя газообразные побочные продукты.
- Образуют первичные спирты в своем сплаве с гидридом лития и алюминием.
Производство
Карбоновые кислоты образуются в результате окисления из первичных спиртов c добавлением перманганата калия:
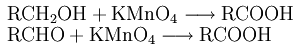
Гидролиз («омыление») сложных эфиров:
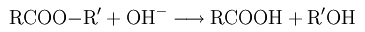
Окисление олефинов перманганатом калия:
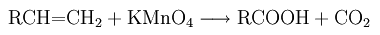
Применение карбоновой кислоты
Карбоновые кислоты и их соли служат пищевыми добавками и являются промежуточными продуктами для многих других веществ и групп веществ в органической химии, например, при производстве ароматизаторов, пластиков, лекарств или красителей.
Пищевая промышленность:
Добавки, консерванты (сорбиновая и бензойная кислоты), регулятор щелочности, антимикробный агент, подкислитель в безалкогольных напитках.
Основной элемент при созревании швейцарского сыра (пропионовая кислота), приготовления квашеной капусты и безалкогольных напитков (молочная кислота).
Фармакология:
Жаропонижающие и анальгетики (ацетилсалициловая кислота), противогрибковые препараты (бензойная кислота), витамин С (аскорбиновая кислота), фунгициды (каприловая кислота).
Другие применения:
- изготовление пластмасс,
- смазки (сорбиновая кислота),
- лаки,
- прозрачные клеи (акриловая кислота),
- краски (линолевая кислота),
- зубная паста (салициловая кислота),
- красители (метановая кислота),
- парфюмерия (бензойная кислота),
- полиэстер (терефталевая кислота),
- парафиновые свечи (стеариновая кислота).
Мыло, моющие средства, косметика, чистящие средства (олеиновая кислота), ароматический синтез, масла (бутановая кислота), фотопленки, фиксаторы цвета (уксусная кислота).
В своей простейшей и наиболее естественной форме эти кислоты содержатся в уксусе (уксусная кислота) и в веществе, вводимом муравьями и пчелами при укусе (муравьиная кислота).
Преимущества карбоновых кислот
Являются частью большого количества клеток организма, составляющих фосфолипиды и триацилглицериды, которые являются жирными кислотами, содержащимися в клеточных мембранах, нейронах, сердечной мышце и нервной ткани.
Присутствуют в фундаментальных процессах, таких как метаболический цикл клеток организма, называемый циклом Кребса.
Биотин в форме карбоновой кислоты участвует в метаболизме углеводов и некоторых аминокислот в качестве фактора роста.