Толуол (метилбензол, фенилметан) представляет собой бесцветную летучую жидкость с характерным запахом, которая по многим своим свойствам похожа на бензол. Толуол — ароматический углеводород, которым часто заменяют токсичный бензол в качестве растворителя.
В 1844 году толуол впервые получил Анри Этьен Сент-Клер Девиль путем сухой перегонки из толуанского бальзама, который и дал название новому веществу.
Получение
В промышленности толуол получают в основном из нефти. Мировое производство составляет от пяти до десяти миллионов тонн в год. Прямое производство из сырой нефти или путем сухой перегонки каменного угля не является экономичным при текущих ценах на сырую нефть. Вот почему его получают при переработке нефти путем крекинга или дегидроциклизации н-гептана :
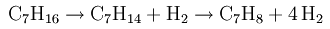
Гептан превращается в метилциклогексан, а затем дегидратируется в толуол.
Свойства
Толуол является самым простым представителем алкильных бензолов. На воздухе горит желтым, сильно коптящим пламенем. Жидкость имеет характерный резкий “приятный” запах (похожий на бензол). Толуол плавится при 95 C, кипит при 111 C и при нормальных условиях представляет собой бесцветную прозрачную жидкость белого цвета, обладающую высокой преломляющей способностью.
В воде практически не растворяется (0,47 г / л), но смешивается в любых пропорциях с сероуглеродом, спиртом, эфиром, хлороформом, ацетоном и большинством других органических растворителей. Теплотворная способность — 40 940 кДж / кг, температура воспламенения 535 C.
Толуол стабилен и относительно инертен при нормальных условиях, но он бурно реагирует с окислителями и кислотами. Аналогично реагирует с фенолом и бензолом, его реакционная способность находится между этими двумя соединениями. Толуол разрушает многие пластмассы и поэтому обычно хранится в стеклянных или металлических контейнерах.
Путем окисления (например, кислым раствором перманганата калия) толуол можно превратить в бензойную кислоту через бензиловый спирт и бензальдегид.
Поскольку толуол относительно инертен, реакции электрофильного замещения протекают относительно медленно, но в присутствии подходящего катализатора скорость реакции может быть значительно увеличена.
Толуол реагирует с азотной кислотой с образованием нитротолуола и воды. Собственно нитрующий агент (NO 2 +) образуется из азотной кислоты в присутствии серной кислоты. Другой важной реакцией является окисление толуола до бензойной кислоты.
Выбросы в окружающую среду
Толуол выделяется автотранспортными средствами, в том числе потому, что он содержится в бензине, а также вырабатывается в небольших количествах, когда органические вещества не сгорают полностью, например, при курении. Основным фактором выбросов толуола в окружающую среду является автотранспорт (около 65 процентов), 33 процента связаны с использованием продуктов, содержащих толуол, и 2 процента с самим производством толуола. Выделяющийся толуол разрушается в земной атмосфере, как и бензол, через несколько дней в результате реакций с гидроксильными радикалами.
Правила техники безопасности
Сам по себе толуол не является мутагенным, но он часто загрязнен бензолом. Более низкая токсичность толуола по сравнению с бензолом может быть объяснена его метаболизмом. В отличие от бензола, толуол практически не метаболизируется до бензойной кислоты за счет окисления кольца, а в основном за счет окисления боковой цепи.
По этой причине практически не образуется канцерогенный эпоксид, как в случае с бензолом.
Толуол и небольшое количество о-крезола выводятся с мочой в виде бензойной кислоты и гиппуровой кислоты.
Толуол вызывает повреждение нервов, почек и, возможно, печени. Толуол токсичен и тератогенен. Вдыхание паров толуола может привести к неспецифическим симптомам, таким как усталость, недомогание, сенсорные нарушения, нарушения координации движений и потеря сознания.
Воздействие толуола на здоровье