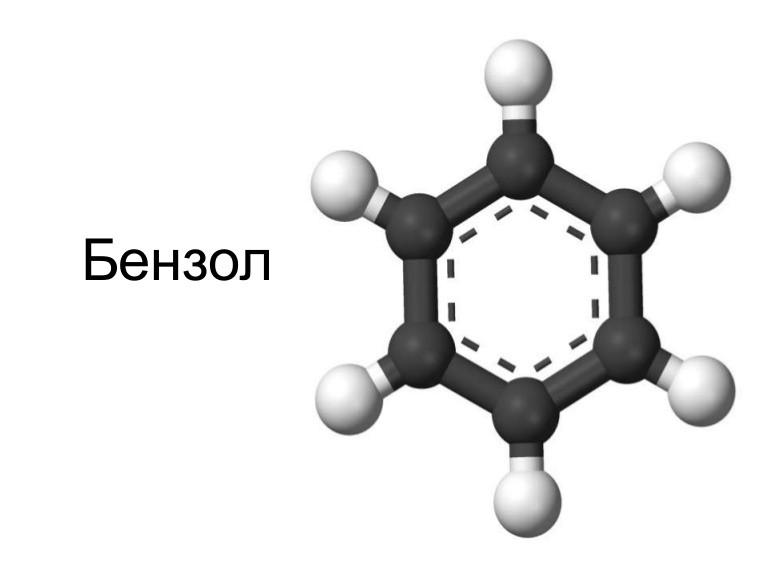
История
Во второй половине 17 века бензол был открыт Иоганном Рудольфом Глаубером, который также открыл глауберову соль при перегонке каменноугольной смолы. Однако полученный состав был ему неизвестен, поэтому он назвал его «нежным и прекрасным олеумом». В 1825 году английский физик Майкл Фарадей выделил это масло из жидких остатков, которые отделились от газовой фазы, когда китовый жир сжигали в лондонских уличных фонарях. В 1834 г. немецкий химик Эйльхард Мицчерлих получил бензол из бензойной кислоты и оксида кальция, а также преобразовал бензол в нитробензол и бензолсульфоновую кислоту. Он назвал это вещество «бензином» из-за его родства с бензойной кислотой. Кроме того, он создал правильную эмпирическую формулу C6H6. В 1845 году английский химик Чарльз Мэнсфилд выделил бензол из каменноугольной смолы, работая под руководством Августа Вильгельма фон Хофмана.
Возник долгий научный спор о правильной структурной формуле бензола. Первоначальные предложения, такие как призматическая структура Джеймса Дьюара, оказались ошибочными. Лишь в 1861 году австрийский школьный учитель Иоганн Йозеф Лошмидт сформулировал некоторые возможные структурные формулы бензола, которые немецкий химик Август Кекуле предложил в 1865 году в качестве предложения для структурной формулы. По легенде, эта идея пришла Кекуле во сне. В этом сне змеи по очереди кусали свои хвосты, создавая кольцевую структуру.
В 1872 году Кекуле сформулировал свою колебательную гипотезу о постоянном изменении одинарных и двойных связей. Только в 20 веке феномен делокализованных электронных облаков, которые придают молекуле бензола особую стабильность, можно было продемонстрировать с помощью рентгеноструктурного анализа.
Промышленное производство бензола из каменного угля началось в 1849 году.
Структурная формула
Бензол в определенной степени является прототипом всех ароматических соединений. Его необычное поведение для соединения, которое на самом деле должно содержать двойные связи, сделало выяснение его структуры одной из основных проблем в химии XIX века.
В 1865 году химику Августу Кекуле, наконец, удалось составить структурную формулу.
Каждый атом углерода имеет четыре валентных электрона, два из которых соединяют атом с соседними атомами углерода. Электрон связывает атом водорода. Остальные шесть электронов формально образуют три π-связи, что выражается двойными связями в структурной формуле. В орбитальной модели, шесть π-электронов скорее образуют облако делокализованных зарядов (делокализованная 6π-электронная система) выше и ниже уровня углеродного кольца. Кекуле выразил этот факт мезомерии двумя структурными формулами, каждая из которых символизирует только одну крайнюю точку зарядового облака. Из-за мезомерии углеродное кольцо более стабильно, чем гипотетический циклогексатриен с локализованными двойными связями, то есть с двойными связями в фиксированных положениях. В упрощенных обозначениях углеродное кольцо теперь представлено в виде шестиугольника, а электронное облако — в виде вписанного круга. Бензол — простейшая незаряженная ароматическая молекула.
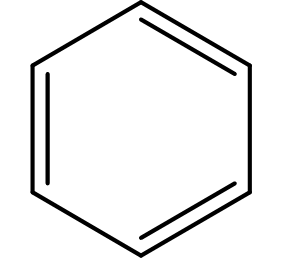
Таким образом, бензол представляет собой равностороннее гексагональное кольцо, состоящее из 6 атомов углерода, все из которых являются вторичными и каждый имеет атом водорода. Однако подробные обозначения обычно опускаются:
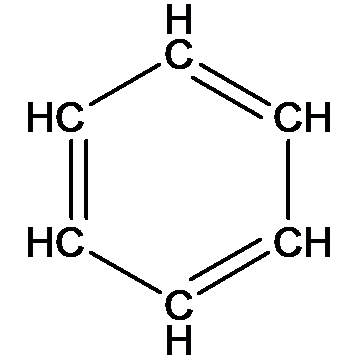
Однако эта структура не объясняет специфического поведения бензола в реакции. Поэтому предполагалось, что сопряженные двойные связи подвержены постоянной миграции, то есть «не находятся в одном месте»:
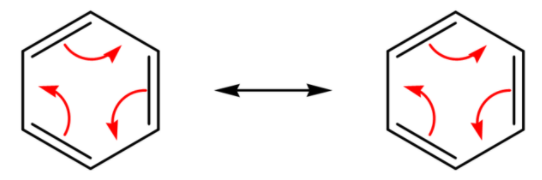
Переворот π-электронов называется мезомерией и характерен для ароматических систем, но не ограничивается ими. Снимок таких мезомерных перестроек называется мезомерной граничной структурой.
В случае дизамещенных продуктов, в зависимости от положения заместителей, различают
- орто (заместитель на атоме углерода 1 и 2);
- мета (заместители на атомах углерода 1 и 3 или 1 и 5);
- пара (заместители на атомах углерода 1 и 4) положения заместителей.
Свойства
Физические свойства
Бензол — бесцветная, прозрачная, летучая и легко воспламеняющаяся жидкость. Показатель преломления бензола довольно хорошо согласуется с показателем преломления оконного стекла, поэтому стекло, погруженное в бензол, практически не видно. Вязкость бензола ниже, чем у воды. Он замерзает при 5,5 градуса Цельсия и закипает при 80,1 градусе Цельсия. При комнатной температуре (20 градусов Цельсия) он имеет плотность 0,88 килограмма на литр.
Бензол хорошо растворим в неполярных органических растворителях, таких как эфир и спирт, но плохо в воде (максимум 1,7 грамма на литр).
Химические свойства
Бензол горит желтым пламенем с образованием воды и углекислого газа, причем сильное образование сажи указывает на высокое содержание углерода в соединении. Теплотворная способность бензола составляет 40 580 кДж на килограмм, энтальпия сгорания составляет 3257,6 кДж на моль для жидкого бензола и 3301 кДж на моль для газообразного бензола. Бензол имеет очень характерный запах. Порог запаха очень низкий и составляет от 1,5 до 900 миллиграммов на кубический метр воздуха.
Важным (узнаваемым) признаком является отсутствие реакции присоединения с бромистоводородной кислотой или бромной водой. Повышение реакционной способности по отношению к добавлению бромистого водорода в ряду четырех структурно подобных соединений циклогексана, циклогексена, циклогексадиена предполагает еще большую реакционную способность бензола, потому что в первых трех соединениях увеличение реакционной способности вызвано может быть определено более высокое количество двойных углеродных связей. В бензол не добавляется бромистоводородная кислота из-за его особой ароматической стабильности, которая возникает в результате делокализации электронов.
Опасность и меры предосторожности
Бензол легко воспламеняется. Пары бензола ядовиты при вдыхании, симптомы острого отравления проявляются только при относительно высоких концентрациях. Легкое отравление проявляется головокружением, тошнотой, сонливостью и апатией. Тяжелое отравление приводит к повышению температуры и нарушению зрения, вплоть до временной слепоты и потери сознания. Так называемая бензольная зависимость, которая может возникнуть при вдыхании бензола, приводит к чувству опьянения и эйфории. Бензол может быть смертельным при длительном воздействии.
Длительное употребление небольшого количества бензола в основном приводит к повреждению внутренних органов и костного мозга. Последнее приводит к снижению количества эритроцитов (анемия), что проявляется в сердцебиении, мерцании глаз, усталости, головокружении, бледности и головной боли. Бензол хранится в головном мозге, костном мозге и жировой ткани, медленно выводится через почки. Острая летальная доза (пероральная) для человека составляет 50 миллиграммов на килограмм. Бензол образует взрывоопасные смеси при объемной долей воздуха от 1,4 до 8%.
С бензолом следует обращаться с особой осторожностью, хранить при температуре от 15 C до 25 C.
Выбросы бензола
Бензол содержится в каменноугольной смоле и нефти. При курении сигарет выделяются небольшие количества паров бензола (10–100 мкг на сигарету), а также следы бензола образуются во время извержений вулканов и лесных пожаров. Половина бензола, присутствующего в атмосфере, разлагается через два-пять дней, поскольку он вступает в реакцию с гидроксильными радикалами (свободными группами ОН). Неполное сгорание органических материалов также приводит к образованию бензола, но в основном бензол выделяется из бензина через выхлопные газы (75% выбросов).
Производство
Бензол можно получить путем крекинга бензина или нефти. В большинстве случаев гексан дегидрируется до циклогексана, а затем до бензола. Другой способ получения бензола — термическое деалкилирование. Метильная группа используемого толуола отделяется при 780 градусах Цельсия и давлении 40 бар. Газ-носитель в реакторе на 90% состоит из водорода. После охлаждения, разделения газа и жидкости и очистки получают чистый бензол. Бензол также можно получить из молекул этина в присутствии катализатора.
Ежегодно во всем мире производится около 35 миллионов тонн бензола.
Производные бензола и важные заместители
В основе многих важных химических веществ лежит бензольное кольцо. К ним относятся, например:
Алкильные заместители:
- Метилбензол — толуол (растворитель)
- Диметилбензол (смесь изомеров) — ксилол (растворитель)
- 1,3,5-триметилбензол — мезитилен (растворитель)
Другие функциональные группы:
- Гидроксильная группа (-ОН), фенол (антисептик)
- Аминогруппа (-NH 2 ), анилин (для производства красителей)
- Алкоксигруппа (-OC n H 2n), анизол (в парфюмерии)
- Алкены (-C n H 2n-1 ), стирол (важный мономер для производства пластмасс и синтетических смол)
Использование
Сам бензол в прошлом часто использовался в качестве растворителя в химической промышленности, но теперь он в значительной степени заменен менее канцерогенными веществами — толуолом и ксилолом. Кроме того, из-за его легковоспламеняющихся свойств его добавляют в моторное топливо, что объясняет, почему 75% бензола в воздухе образуются из-за выбросов автомобилей.
В виде производных, таких как толуол, анилин или фенол, он используется в промышленности для производства текстиля, парфюмерии, фармацевтических препаратов, пластмасс и красителей. Ацетилсалициловая кислота и парацетамол также содержат бензольный каркас.
Воздействие бензола на здоровье