Этанол (общее название спирт) представляет собой алифатический одноатомный спирт с молекулярной формулой C2H6O. Чистое вещество представляет собой бесцветную, легко воспламеняющуюся жидкость при комнатной температуре с жгучим вкусом и характерным пряным (сладковатым) запахом. Спирт в основном известен как составная часть стимуляторов и алкогольных напитков, таких как вино, пиво и ликер.
Ферментация из сахара в этанол является одним из старейших известных биохимических реакций. Спирт широко используется в качестве растворителя для веществ, используемых в медицинских или косметических целях, таких как ароматизаторы, красители, лекарства, дезинфицирующие средства. Химическая промышленность использует его как в качестве растворителя, так и в качестве сырья для синтеза других продуктов, таких как этиловые эфиры карбоновых кислот.
В последние десятилетия этанол стал активно использоваться в качестве биотоплива (биоэтанола).
Описание
Этанол (C2 H5 OH) относится к линейным алканолам. «Алкоголь или спирт» является устоявшимся разговорным обращением. Термин «спирты» обозначает группу органических химических соединений, которые, в дополнение к углеводородному скелету, имеют по меньшей мере одну гидроксильную группу в качестве дополнительной функциональной группы. При этом у атома углерода, содержащего гидроксильную группу, отсутствует заместитель более высокого порядка.
Спирт является естественным продуктом алкогольного брожения в зрелых фруктах и соках. Многие продукты содержат небольшое количество этанола. Например, безалкогольное пиво содержит до 0,5%. Фруктовые соки могут иметь содержание спирта около 0,38%. Исключением является виноградный сок, который может содержать до 1% этанола, также как спелый банан и кефир. Физиологическое содержание спирта в крови человека составляет от 0,02 до 0,03%.
История
Этанол естественным образом образуется при ферментации сахаристых фруктов. Человек издревле использовал это природное вещество для опьянения и одурманивания. Пиво, а позднее и вина были впервые произведены с помощью природных дрожжей. Содержание спирта в таких напитках было ниже, чем сегодня, потому что природные дрожжи прекращают превращать сахар в этанол при достижении определенной концентрации. Современные культивированные дрожжи позволяют достичь более высоких концентраций.
В 1796 году Иоганн Тобиас Лоуиц впервые получил чистый этанол путем фильтрации дистиллированного спирта через активированный уголь. Антуан Лавуазье впервые описал этанол как соединение углерода, водорода и кислорода. В 1808 году Николя-Теодор де Соссюр определил химический состав. Пятьдесят лет спустя Арчибальд Скотт Купер опубликовал структурную формулу. Синтетически спирт был впервые произведен в 1826 году Генри Хеннелем и Джорджем Саймоном Серуллой в Соединенном Королевстве Великобритании.
Сегодня этанол в основном получают путем ферментации из биомассы. В контексте производства биотоплива его называют биоэтанолом. Сельскохозяйственный спирт — это этанол из сельскохозяйственного сырья.
Производство
Ферментация
Этанол получают путем ферментации из биомассы, обычно из сахарных или крахмалосодержащих культур, или традиционно из садовых фруктов и овощей. Этот процесс осуществляется контролируемым образом с использованием ряда пищевых продуктов, например, вина из винограда или пива из солода и хмеля.
Крахмалосодержащее сырье (картофель и злаки) должно быть предварительно обработано для производства сбраживаемого сахара. Во время ферментации крахмал сначала расщепляется на дисахариды, гликозидные связи которых расщепляются гидролазами. Полученные моносахариды затем ферментируются дрожжами или бактериями. При концентрации этанола около 15% дрожжевые клетки и бактерии начинают умирать, что означает, что ферментация не может достичь более высокой концентрации. Общее уравнение алкогольного брожения:

Дистилляция
Питьевой спирт получают путем перегонки алкогольного сусла из сельскохозяйственного сырья. В зависимости от процесса сгорания дистиллят содержит ароматизаторы, сивушные масла и другие органические соединения, которые определяют характер и вкус конечного продукта, такого как бренди, виски или ром. Для производства водки используется почти чистый этанол, разбавленный только водой. Чистый спирт используется неразбавленным в качестве исходного материала для других алкогольных напитков, например, для большинства ликеров.
Алкогольные напитки, содержащие дистиллированный этанол, называются спиртными напитками — в отличие от вина и пива, этанол которых производится исключительно путем алкогольной ферментации.
Технический синтез
Этанол получают химическим синтезом из воды и этена в так называемом косвенном гомогенном каталитическом процессе с добавлением серной кислоты. Процесс проводится в две стадии с образованием сложных эфиров серной кислоты, которые должны быть гидролизованы на второй стадии. Серная кислота должна быть повторно сконцентрирована после гидролиза. В прямом процессе фосфорная кислота, нанесенная на кремнезем, действует как гетерогенный катализатор. Из-за проблем сточных вод и коррозии, вызванных использованием серной кислоты, в настоящее время этанол производится в промышленности путем катализа фосфорной кислоты. Общее уравнение для обоих процессов:

Физические свойства
Отличительной особенностью спирта является его гидроксигруппа. Поскольку атом кислорода притягивает электроны больше, чем водород и углерод, то вдоль этой связи возникает асимметричное распределение электронной плотности — образуется молекулярный диполь. С одной стороны, диполи взаимно притягивают друг друга на молекулярном уровне, что приводит к сравнительно высокой температуре кипения — 78 С, а с другой стороны, этанол смешивается с жидкостями, которые имеют сходные дипольные свойства, например, вода и метанол. Это свойство называется гидрофильностью. По этой причине этанол является важным растворителем в химии и фармакологии. Растительные экстракты или другие лекарства в виде спиртовых растворов называются «настойка».
Спирт смешивается с водой в любых пропорциях. При смешивании с выделением тепла происходит сокращение объема. Общий объем смеси вода / этанол меньше суммы отдельных объемов. Смешивая 50 мл этанола с 50 мл воды, получится 97 мл этанол-водной смеси.
В органических растворителях, таких как четыреххлористый углерод, этанол образует димеры, тримеры и тетрамеры в зависимости от концентрации.
Химические свойства
Этанол растворяется в любых пропорциях с водой и многими другими органическими растворителями, такими как диэтиловый эфир, хлороформ и бензол.
Эстерификация
Катализируемый кислотой этанол реагирует с карбоновыми кислотами с образованием этиловых эфиров:
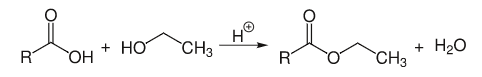
Этиловые эфиры используются в качестве добавок для косметики и ароматизаторов.
Обезвоживание
Очень сильные кислоты, такие как серная кислота, катализируют дегидратацию спирта. В процессе образуется диэтиловый эфир или этилен:
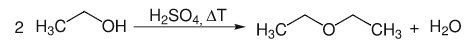
Этанол расщепляет воду в реакции элиминации с образованием двойной связи.
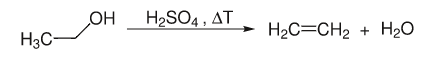
Окисление
Этанол может быть окислен из атмосферного кислорода при комнатной температуре через ацетальдегид в уксусную кислоту. В лаборатории сильные неорганические окислители, такие как хромовая кислота или перманганат калия, служат для окисления спирта до уксусной кислоты.
На воздухе этанол горит синим пламенем с теплотворной способностью около 30 МДж / кг с образованием углекислого газа и воды:

С помощью хлора или брома этанол вступает в реакцию с ацетальдегидом. Это формирует полуацетали. Дальнейшее окисление хлором приводит к гемиацеталию хлорала. В реакции с тионилхлоридом образуется этилхлорид.
Применение
Основная часть произведенного этанола используется для производства различных алкогольных напитков. Он также служит в качестве растворителя для потребительских товаров (духи, дезодоранты) и медицинского использования (растворитель для лекарственных средств, дезинфицирующих средств).
Спирт используется в качестве чистящего средства для стекла, хрома, пластика. Применяется в качестве стеклоомывателя, пятновыводителя и антифриза.
Этанол используется в различных реакциях этерификации. Полученные сложные эфиры используются в качестве растворителей и промежуточных соединений для последующих синтезов. Важным вторичным продуктом является этилакрилат — мономер, используемый в качестве сомономера в различных процессах полимеризации. Этилацетат в качестве растворителя для клеев и лаков для ногтей. Гликолевые эфиры, такие как 2-этоксиэтанол, широко используются в качестве растворителей для масел, смол, жиров, восков, нитроцеллюлозы и лаков.
Медицина
Эффективность дезинфицирующего или антисептического средства (например, для дезинфекции рук) зависит от концентрации смеси этанол-вода. При оптимальном содержании алкоголя от 50 до 80% все бактерии, включая туберкулезные бактерии, погибают в течение одной минуты путем денатурирования бактериальной клеточной стенки. Но спирт ограничен в эффективности против вирусов и не эффективен против бактериальных эндоспор.
Питьевой этанол или алкогольные напитки не действуют как антисептики. Напитки с содержанием этанола менее 20% практически не убивают микробов.
Спирт играет важную роль в сохранении и стабилизации жидких лекарственных средств растительного происхождения (фитотерапия). Народная медицина использует разбавленные спиртовые растворы для лечения укусов насекомых.
В случае отравления метанолом этанол вводится внутривенно в качестве первой помощи. Этанол ингибирует превращение метанола через фермент алкогольдегидрогеназу в токсичный метанал. Этанол связывает примерно в 25 раз больше алкогольдегидрогеназы, чем метанол.
Удаление плесени
При относительно новом и поверхностном заражении плесенью на гладких материалах, таких как металл, керамика, стекло или лакированное дерево, их достаточно просто очистить губкой с обычным бытовым чистящим средством. Но пористые поверхности, такие как штукатурка, должны обрабатываться 70-80% этиловым спиртом.
Меры по предотвращению появления плесени в доме:
Свежий воздух
Постоянный приток свежего воздуха помогает против образования плесени. Помещение необходимо проветривать минимум 3 раза в день в течение 7-10 минут.
Влага
Плесень чаще всего образовывается при наличии влаги. Влага оседает на поверхности когда стена становится слишком холодной.
Ремонт
Плесень часто возникает, когда в старом доме устанавливаются новые герментичные стеклопакеты. Воздухообмен прекращается, стены охлаждаются, на них осаждается влага и образуется плесень.
Алкогольные напитки и сырье, из которого они производятся
- Вишневый и сливовый бренди (спирт из сброженных вишен или слив)
- Кальвадос (спирт из яблок Франции, регион Кальвадос)
- Текила (напиток из определенного типа агавы)
- Ром (напиток из сахарного тростника)
Вещества, уже содержащие спирт (вино, пиво и остатки от их производства)
- Бренди (спирт из вина)
- Коньяк (бренди из Франции, регион Коньяк)
- Арманьяк (бренди из Франции, регион Арманьяк)
- Кондитерский бренди (напиток из винодельческих остатков)
- Граппа (напиток из Италии)
Крахмалистые вещества или крахмалистое содержимое (крупы, картофель, рис, мука, манная крупа или отруби из них)
- Водка (спирт из пшеницы, кукурузы или картофельного дистиллята)
- Виски (спирт из ячменя, ржи, овса и / или кукурузы)
- Джин (спирт из пшеницы, кукурузы, ржи или ячменя) с добавлением ягод можжевельника и специй)
Влияние на здоровье
Этанол всасывается по всему пищеварительному тракту. Первый этап в небольшой степени начинается уже в слизистой оболочке полости рта. Поглощенный там спирт поступает непосредственно в кровь и, таким образом, распределяется по всему телу, включая мозг. Около 20% всасывается в желудке, остальное в тонкой кишке.
Этанол, абсорбированный в желудке и кишечнике, сначала попадает в печень вместе с кровью, где он частично разлагается. Всасывание спирта увеличивается за счет различных факторов, таких как тепло (ирландский кофе, грог), сахар (ликер) и углекислый газ (игристое вино).
Приблизительно 2-10% выпитого спирта выделяется с мочой, потом и выдыхаемым воздухом.
В печени, основная часть этанола (как и другие растворимые в воде токсины) с помощью ферментов алкогольдегидрогеназы (АДГ) деградируют спирт до уксусной кислоты. Уксусная кислота затем превращается в CO2 через цикл Кребса. Промежуточный этанал отвечает за так называемые симптомы «похмелья» — головная боль, тошнота и рвота. Разложение этана сдерживается сахаром, поэтому похмелье бывает особенно интенсивно при употреблении сладких алкогольных напитков, особенно ликера и некоторых сортов шампанского.
Скорость деградации алкогольдегидрогеназой является постоянной в определенных пределах. У мужчин это около 0,1 г в час и кг массы тела, у женщин 0,085
Токсикология
Этанол не классифицируется ни как яд, ни как вредный для здоровья элемент. Но патологи считают его «гепатотоксическим веществом», то есть прямым токсином печени. А педиатры называют его «тератогенным ядом», который может поврежить плод.
Излишнее потребление спирта приводит к типичным симптомам острой интоксикации, таким как головокружение, тошнота, дезориентация, разговорчивость и повышенная агрессия. Летальная доза (ЛД) составляет приблизительно от 3,5 до 4,0 промилле.
Другие статьи
ОПИСАНИЕ ЭТИЛОВОГО СПИРТА (ЭТАНОЛ)
ФЕРМЕНТАЦИЯ ФРУКТОВ ДЛЯ ПОЛУЧЕНИЯ СПИРТА
ВЛИЯНИЕ АЛКОГОЛЯ НА ЗДОРОВЬЕ ЧЕЛОВЕКА
ПРОИЗВОДСТВО АЛКОГОЛЯ В ДРЕВНОСТИ







