Синонимы: диоксиянтарная кислота, тартаровая кислота, 2,3-дигидроксибутандиовая кислота, пищевая добавка Е334, wine acid
Фасовка: Мешки по 25кг
Винная кислота представляет собой химическое вещество, которое является незаменимым регулятором кислотности различных продуктов. Данный реагент в основном имеет белый или прозрачный цвет, агрегатное состояние — кристаллический порошок. В настоящий момент винную кислоту получают в основном из винограда, а точнее из его сока. Полученный продукт внешне очень напоминает обычный сахар, однако на вкус винная кислота приятно вяжущая, но не сладкая.
Соли винной кислоты называются тартратами. Винная кислота разрешена в ЕС в качестве пищевой добавки с номером Е334. Путем межмолекулярной дегидратации образуется полимерная метатартаровая кислота, которая используется в качестве пищевой добавки (Е353).
История
Ранее соль винной кислоты — тартрат калия (тартар) принимали за саму кислоту. Так как она легко осаждалась из-за плохой растворимости в воде в вине и ее легче было распознать для первых химиков, чем легко растворимую винную кислоту.
В 1764 году Маркграф обнаружил в тартаре щелочной металл, после чего он разложил его на кальций с образованием тартрата кальция, который он не исследовал более внимательно.
Лишь в 1769 году Шееле, широко известный как первооткрыватель винной кислоты, разложил тартрат кальция с помощью серной кислоты и описал осажденную кристаллическую кислоту.
Изомерия винной кислоты была открыта в 1826 году Гей-Люссаком. Позднее она была более подробно изучена Пастером. В то время были известны только оптически активная «правовращающая винная кислота», то есть L-винная кислота и виноградная кислота, известная как «рацемическая кислота». Пастер приготовил натриево-аммониевую соль этих кислот, открыв тем самым хиральность. С помощью лупы и пинцета Пастер осторожно разделил кристаллы на две части, левовращающиеся и правовращающиеся.
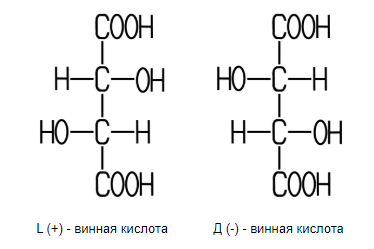
Полученные таким образом из рацемата энантиомерные тартраты натрия-аммония были повторно растворены Пастером и исследованы в поляриметре. Он обнаружил, что оба раствора солей были активными и имели такое же удельное вращение как натриево-аммониевая соль, полученная из L-винной кислоты, но вращение в одном из двух растворов имело противоположный знак.
Однако интерпретации эксперимента Пастера отнюдь не исчерпываются наблюдением, что рацемическая кислота является рацематом L- и D-винной кислоты. Хотя Пастер уже признал, что оптическая активность должна быть следствием свойства самой молекулы винной кислоты. Но только в 1874 году Ле Бел и Вант Хофф, которые впоследствии стали первыми Нобелевскими лауреатами по химии, смогли объяснить независимо друг от друга молекулярную структуру винной кислоты.
Предположив, что «четыре разных объекта могут быть расположены двумя разными способами в углах тетраэдра в зеркальном отражении».
Основываясь на этой гипотезе, они предположили, что оптически активные молекулы содержат, по крайней мере, один асимметричный атом углерода. «Оптически неактивные органические вещества либо не содержат асимметричного атома углерода, либо представляют собой смеси равных частей двух энантиомеров».
Вант Хофф и Ле Бел описали тетраэдрическую геометрию атома углерода и дали убедительное объяснение оптической активности. Долгое время неизвестно, какой энантиомер винной кислоты вращается вправо, а который влево.
Лишь в 1951 году Бийвоет смог использовать специальный рентгеновский метод, основанный на тартрате рубидия натрия, чтобы объяснить, что L-винная кислота является правовращающим (+) энантиомером, а D-винная кислота является левовращающим (-) энантиомером.
Нахождение
L (+) винная кислота и ее соли кальция, калия и магния в изобилии содержатся в лозах, винограде и листьях, а также в одуванчиках, сахарной свекле, листьях агавы, черного перца, ананаса и многих других фруктов. В виноделии труднорастворимые соли винной кислоты осаждаются в виде винного камня на дно бочек или винных бутылок. D (-) винная кислота, также называемая неестественной винной кислотой, встречается только в листьях западноафриканского дерева Bankinia reticulata.
Области применения
Прежде чем купить винную кислоту, необходимо ознакомиться со сферами ее использования.
Пищевая промышленность. Наиболее очевидным применением винной кислоты является ее использование в качестве пищевой добавки. L-винная кислота (Е 334) не только естественным образом содержится во многих продуктах, но также искусственно добавляется во многие продукты благодаря своим вкусовым и консервирующим свойствам.
Винная кислота используется в приготовлении мороженого, искусственного меда, фруктов, газированных и безалкогольных напитков, желе, жевательных и кондитерских изделий, а также в подкислении вин.
Оптовые поставки винной кислоты могут решить многие проблемы пищевой промышленности, главной из которых считается краткий срок хранения некоторых продуктов. Использование винной кислоты значительно повышает срок хранения продуктов. При этом, не вредя здоровью потребителей.
Виноделие. Винная кислота является основой для многих винных напитков. Также данное химическое вещество может использоваться в кондитерской промышленности взамен коньяка и прочих алкогольных напитков, применяемых для изготовления некоторых видов теста.
Косметология. Винная кислота может быть использована как основа для изготовления различных косметологических средств, которые в дальнейшем могут быть использованы для ухода за кожей лица. Винная кислота повышает регенерацию кожи, а также способствует её омоложению и значительно замедляет процесс старения кожи лица.
Фармацевтика. Винная кислота является незаменимым составляющим разнообразных шипучих лекарственных средств, она не только позволяет конечному продукту моментально растворяться, но и придает раствору приятные вкус, что особенно важно при производстве детских лекарственных препаратов.
Текстильное производство. В данной сфере винная кислота применяется в процессе крашения некоторых тканей. Она позволяет не только равномерно нанести цвет, но и препятствует его дальнейшему выгоранию, выцветанию и вымыванию.
Аналитическая химия. В химической промышленности и учебных заведениях винная кислота является незаменимым элементом в процессе синтеза разнообразных солей, а также для получения кислотных эфиров и тартратов.