Перманганат калия (KMnO4) представляет собой калиевую соль перманганцевой кислоты.
Характеристики
Перманганат калия образует темные красно-фиолетовые блестящие кристаллы, которые умеренно растворимы в воде и даже при низких концентрациях образуют раствор ярко-фиолетового цвета. При нагревании кристаллы не плавятся, а распадаются с отчетливым треском, выделяя кислород. Кристаллический перманганат калия стабилен при комнатной температуре, но его водные растворы со временем разлагаются.
Поскольку марганец находится в наивысшей степени окисления в перманганат-анионе, он выступает в качестве очень сильного окислителя в окислительно-восстановительных реакциях. Например, перманганат калия окисляет соляную кислоту до газообразного хлора (лабораторный метод получения хлора):
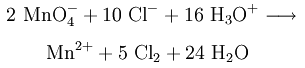
Также окисляет, например, сульфиты до сульфатов, Fe (II) до ионов Fe (III) и спирты до карбоновых кислот. Перманганат калия разлагается при температуре 240 C на диоксид марганца (MnO2), оксид калия (K2O) и кислород (O2):
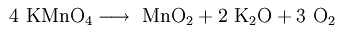
Благодаря своему окислительному эффекту, перманганат калия окрашивает кожу, текстиль и древесину в коричневый цвет.
Производство
Производство происходит в лаборатории с использованием двухстадийного синтеза, при котором диоксид марганца сначала окисляется в сильно щелочной среде с помощью хлорида калия, а затем превращается в перманганат калия. Таким образом, перманганат калия получают синтетическим путем из калиевой соли пермангановой кислоты с чистотой 99,1% в виде порошка. В качестве сырья для производства используется диоксид марганца. Вместе с гидроксидом калия и кислородом он реагирует с образованием манганата калия характерного зеленого цвета.
Техническое производство основано на диоксиде марганца MnO2, который реагирует с гидроксидом калия и атмосферным кислородом с образованием манганата калия (VI). Затем с помощью электрохимического процесса получается перманганат калия (анодное окисление).
Применение
Перманганат калия часто используется в качестве окислителя в синтезе и органических реакциях. Он также используется при очистке воды для удаления марганца или для обратной промывки систем фильтрации.
Из-за сильного окислительного эффекта перманганат калия используется, среди прочего, как дезинфицирующее средство, дезодорант и альгицид. В количественном химическом анализе (оксидиметрия, окислительно-восстановительное титрование) он используется для определения большого количества веществ (например, железа и косвенно кальция). В лаборатории щелочной раствор перманганата калия используется для очистки стеклянных приборов.
В фотографии применяется для обнаружения фиксирующей соли (тиосульфата натрия). Ранее фотографы использовали перманганат калия в качестве ингредиента порошка для вспышки.
В медицине раствор перманганата калия используется как вяжущее и дезинфицирующее средство для наружной обработки кожи, для лечения микозов стопы или опрелостей. В токсикологии раствор перманганата калия бордового цвета (около 0,1%) используется для промывания желудка в случае отравления после перорального приема окисляющихся ядов.
Перманганат калия также используется:
- для борьбы с вредителями в органическом земледелии;
- для борьбы с грибками и бактериями на фруктовых, оливковых деревьях и виноградных лозах;
- для борьбы с паразитами и микробами в карповых прудах;
- для производства подсластителя;
- в ветеринарии при паразитарных болезнях рыб.
Правила техники безопасности
Из-за сильных окислительных свойств при обращении с перманганатом калия необходимо соблюдать определенные инструкции по безопасности, чтобы при его смешивании с порошком магния или алюминия не возникло ущерба окружающей среде, химического ожога или даже взрыва. Также наблюдается самовоспламенение вместе с ацетальдегидом, этиленгликолем и глицерином.
Перманганат калия очень опасен для воды и при неправильном использовании может нанести вред окружающей среде, поскольку его окислительный эффект убивает организмы и может вызвать химические ожоги слизистых оболочек и обесцвечивание кожи. Перманганатная пыль может затуманивать роговицу.
Перманганат калия имеет низкую острую токсичность, но оказывает выраженное раздражающее действие на живые ткани из-за своего сильного окислительного действия. Поэтому следует избегать любого контакта, выходящего за рамки медицинского применения или даже перорального приема! При попадании в глаза перманганатная пыль вызывает помутнение роговицы.
Как правильно хранить перманганат калия?
Перманганат калия необходимо хранить в закрытых шкафах, защищенных от прямых солнечных лучей. Открытые контейнеры должны быть плотно закрыты после использования.
Избегать хранения вместе с другими горючими химическими веществами! Шкафы должны быть заперты, чтобы они были недоступны для детей.
Остатки перманганата калия не должны попадать в грунтовые воды!







