Свойства
- Температура плавления: -35 С
- Температура кипения: 83 C
- Плотность: 1,256 г / мл при 25 C
- Физическое состояние: Жидкость
- Растворимость в воде: 8,7 г / л (20 C)
Химические свойства
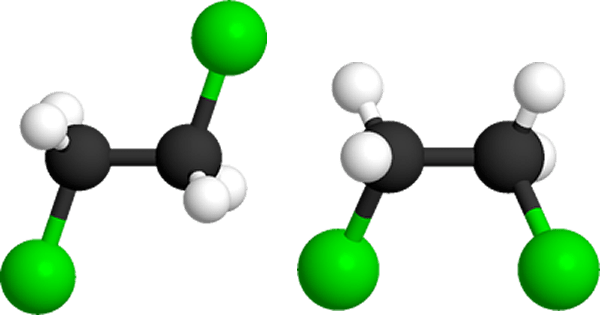
Этилендихлорид — бесцветная маслянистая жидкость с запахом хлороформа, обнаруживаемым в диапазоне 6-40 частей на миллион. Этилендихлорид (1,2-дихлорэтан) имеет одинарную связь углерод-углерод. Следует отличать от 1,2-дихлорэтилена, который имеет двойную связь углерод-углерод.
Физические свойства
Прозрачная бесцветная маслянистая жидкость с характерным запахом хлороформа. Средние пороговые концентрации наименее обнаруживаемого запаха в воде при 60 C и в воздухе при 20 C составляют 12 и 52 мг / л соответственно.
Применение
Самым большим применением является производство мономера винилхлорида, который используется для производства поливинилхлорида (ПВХ).
Другие применения включают в себя:
- средства для удаления краски, лака;
- в качестве растворителя для резины, табачного экстракта;
- при производстве ацетилцеллюлозы;
- при производстве мыла и чистящих средств;
- при производстве смачивающих и проникающих агентов;
- в качестве диспергатора для нейлона, вискозы, бутадиен-стирольного каучука;
- в качестве добавки к бензину (используется как поглотитель свинца).
Получение
№1
Процесс получения EDC начинается с сырой нефти или природного газа и хлорида натрия. Углеводородное сырье превращается в этен (этилен), а хлорид натрия подвергается электролизу с образованием хлора.
2 NaCl + 2 H2O = Cl2 + 2 NaOH + H2
Этот электрохимический процесс также является основным промышленным способом получения гидроксида натрия, поэтому, по существу, единственным побочным продуктом этой начальной реакции является газообразный водород, который позже превращается в воду. После того, как этилен получают из сырых углеводородов, он вступает в реакцию с газообразным хлором
№2
В результате реакции этилена и хлора в присутствии хлорида железа (III).
Опасность
Пары дихлорэтана тяжелее воздуха и могут распространяться по земле. Вещество разлагается при разогреве и сжигании с образованием токсичных и едких паров, в том числе хлористого водорода и фосгена. Реагирует бурно с алюминием, щелочными металлами, амидами щелочных металлов, аммиаком, основаниями и сильными окислителями. Агрессивен в отношении многих металлов и пластиков.
Помощь при отравлении дихлорэтаном
В случае 1,2-дихлорэтана, помимо вдыхания, необходимо учитывать также его быстрое всасывание через кожу. В высоких концентрациях он раздражает глаза, дыхательные пути и может вызвать повреждение легких. Острое воздействие обычно влияет на центральную нервную систему, вызывая головную боль, головокружение, сонливость и даже кому.
Вынести пострадавших из опасной зоны на свежий воздух. При затрудненном дыхании дать кислород.
Если дыхание остановилось, проведите реанимацию «рот в нос», если это невозможно, используйте реанимацию «рот в рот». Следите за чистотой дыхательных путей.
В случае остановки сердца (отсутствие реакции зрачков и дыхания) немедленно выполните компрессию грудной клетки и искусственное дыхание. По возможности используйте дефибриллятор. Всегда как можно скорее обращайтесь за медицинской помощью.